硫化钠水解(硫化钠水解离子浓度大小比较)
硫化钠水解方程式
1、硫化钠水解方程式是:Na2S+H2O=NaHS+NaOH。化钠又称臭碱、臭苏打、黄碱、硫化碱。硫化钠为无机化合物,纯硫化钠为无色结晶粉末。吸潮性强,易溶于水。水溶液呈强碱性反应。触及皮肤和毛发时会造成灼伤。故硫化钠俗称硫化碱。
2、硫化钠和解方程式,硫化钠水解Na2S+H2O=NaHS+NaOH 或者S2- +H2O=HS- +OH-;(可逆),钠又叫臭苏打、臭苏打、黄苏打、硫化钠。硫化钠是一种无机化合物,纯硫化钠是无色结晶粉末。吸湿性强,易溶于水。水溶液呈强碱性。
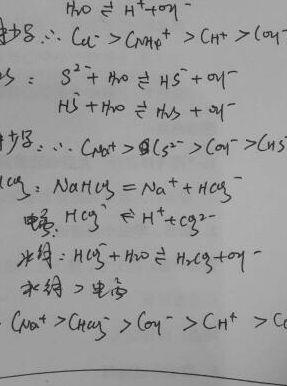
3、硫化钠是一种常见的化学物质,它可以通过水解反应得到硫化氢和氢氧化钠。在这个反应过程中,质子守恒非常重要。当硫化钠溶于水时,其分子会与水分子发生作用,产生硫化氢和氢氧化钠。
4、在Na2S和As2S3的水解中,Na2S的水解较彻底。Na2S是硫化钠,而As2S3是三硫化二砷。当它们与水反应时,会发生水解反应,产生对应的酸和碱。
5、S2- (aq) + H2O (l) HS- (aq) + OH- (aq)这个平衡反应会导致硫化钠的水解不完全电离。部分硫离子会转化为氢硫化物离子,而不是完全转化为硫酸根离子(SO42-)。这是因为氢硫化物离子相对稳定,并且具有较弱的亲水性。
帮我写一下硫化钠的水解方程式。
1、①:水解Na2S+H2O=NaHS+NaOH 或者S2- +H2O=HS- +OH-;(可逆)②:水解NaHS+H2O=H2S+NaOH 或者HS- +H2O=H2S +OH- ;(可逆)(一)硫化钠又称臭碱、臭苏打、黄碱、硫化碱。硫化钠为无机化合物,纯硫化钠为无色结晶粉末。吸潮性强,易溶于水。水溶液呈强碱性反应。
2、硫化钠水解方程式为:Na2S + H2O NaOH + NaHS。硫化钠,也被称为硫化碱,是一种无机化合物,它的水溶液呈现出强碱性。当硫化钠溶解在水中时,它会发生水解反应。水解反应是一种化学反应,其中水分子与另一化合物发生反应,导致该化合物分解并产生新的化合物。
3、硫化钠和解方程式,硫化钠水解Na2S+H2O=NaHS+NaOH 或者S2- +H2O=HS- +OH-;(可逆),钠又叫臭苏打、臭苏打、黄苏打、硫化钠。硫化钠是一种无机化合物,纯硫化钠是无色结晶粉末。吸湿性强,易溶于水。水溶液呈强碱性。
硫化钠和水发生水解反应吗
1、电离:Na2s==2Na++S2-水解:S2-+H2O==HS-+OH-HS-+H2O==H2S+OH-水解程度远小于电离程度。
2、硫化钠与水会发生水解,生成H2S和 NaOH Na2S+2H2O=2NaOH+H2S 当然此水解反应是可逆的。
3、①:水解Na2S+H2O=NaHS+NaOH 或者S2- +H2O=HS- +OH-;(可逆)②:水解NaHS+H2O=H2S+NaOH 或者HS- +H2O=H2S +OH- ;(可逆)(一)硫化钠又称臭碱、臭苏打、黄碱、硫化碱。硫化钠为无机化合物,纯硫化钠为无色结晶粉末。吸潮性强,易溶于水。水溶液呈强碱性反应。
4、你好! 这个是一个水解反应 硫化钠固体遇水 会电离出硫离子 硫离子水解会有硫氢根离子生成;硫氢根离子进一步水解得到硫化氢。
5、硫化碱 (Na2 S· 9H2 O)是一种重要的化工产品,广泛应用于有色金属的选矿和冶金中。
6、硫化钠和解方程式,硫化钠水解Na2S+H2O=NaHS+NaOH 或者S2- +H2O=HS- +OH-;(可逆),钠又叫臭苏打、臭苏打、黄苏打、硫化钠。硫化钠是一种无机化合物,纯硫化钠是无色结晶粉末。吸湿性强,易溶于水。水溶液呈强碱性。
硫化钠水解的质子守恒
硫化钠是一种常见的化学物质,它可以通过水解反应得到硫化氢和氢氧化钠。在这个反应过程中,质子守恒非常重要。当硫化钠溶于水时,其分子会与水分子发生作用,产生硫化氢和氢氧化钠。
解决方案1:消耗一个H+,但是准确性较高:2{[H2S]+[HS-]+[S2-]}=[Na+] (2)去掉[Na+]。
分析:Na2S溶液中的H+来自于H2O,H2O=H+ +OH-,S2-结合掉1个H+会变为HS-,S2-结合掉2个H+会变为H2S,所以质子守恒式如此。
硫化钠的三大守恒是电荷守恒,物料守恒,质子守恒。物料守衡:C(Na+)=2C(S2-)+2C(HS-)+2C(H2S)。电荷守衡:C(Na+)+C(H+)=2C(S2-)+S(HS-)+C(OH-)。质子守衡:C(H+)=C(OH-)-C(HS-)-2C(H2S)。
根据质子守恒水电离的氢氧根浓度等于水电离的氢离子浓度。由于硫离子水解。水电离的氢离子浓度减少,包括硫离子水解生成的硫氢根和生成的硫化氢。
质子守恒就是,水电离出的H+=OH-,水电离出的H+,用去1个H结合1个S2-形成1个HS-,用去2个H+结合S2-形成1个H2。
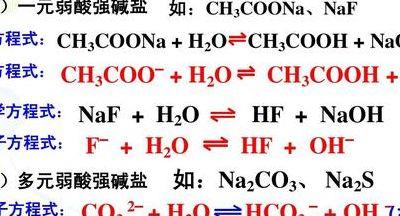
硫化钠水解的离子方程式
硫化钠水解离子方程式为:Na2S+H2O=2NaOH++H2S2(气体)离子方程式 S2-+H2O=OH-+H2S(气体)水解方程 S2-+H2O=HS-+OH-HS-+H2O=H2S+OH-(等号都是可逆的)Na2S为硫化钠,又称臭碱、臭苏打、黄碱、硫化碱。硫化钠水解离子方程式为:S2-+H2O=OH-+H2S(气体)。
(HS-)+H2O=H2S+OH- 第一步水解生成HS-的本身比例就少,第二步反应又靠HS-水解。所以,第二步反应微乎其微。建议还是把第二步写上。写上肯定不会错。
楼上的废话怎么那么多?!人家要离子方程式,你给人家化学方程式,真晕。一楼的也不对,二元离子要分步水解,正确的是:S2- + H2O = HS- + OH- 。绝对对。
电离:Na2s==2Na++S2-水解:S2-+H2O==HS-+OH-HS-+H2O==H2S+OH-水解程度远小于电离程度。